Старение распространяется по организму как инфекция, и виной тому может быть этот белок

СЕУЛ, Южная Корея — Учёные обнаружили молекулярный механизм, объясняющий, как старение клеток распространяется по организму и ускоряет общее старение.
В журнале Metabolism опубликованы результаты исследования, согласно которым белок HMGB1 действует как «сигнальный агент старения». Он чувствителен к окислительно-восстановительным процессам и может передавать сигналы, которые превращают здоровые клетки в старые и нефункциональные. Но это происходит только тогда, когда белок находится в определённом химическом состоянии.
Обычно HMGB1 находится в ядре клеток и помогает организовать ДНК. Однако при стрессе или старении клетки выделяют этот белок в окружающую среду. В зависимости от количества кислорода, с которым контактировал HMGB1 вне клетки, он может существовать в разных химических формах.
Исследователи из Медицинского колледжа Корейского университета выяснили, что только «восстановленная» форма HMGB1 ускоряет старение. Она не подвергалась воздействию большого количества кислорода и может связываться с клеточными рецепторами, активируя процессы старения. Окисленная форма этого не может.
Чтобы подтвердить результаты, учёные провели эксперименты с клетками лёгких, почек, кожи и мышц человека. Клетки, обработанные «восстановленной» формой HMGB1, начали проявлять признаки старения: перестали делиться, выразили маркеры старения (p21 и pи начали выделять воспалительные молекулы. Клетки, обработанные окисленной формой, остались здоровыми и продолжали делиться нормально. Эффект был одинаковым для всех типов

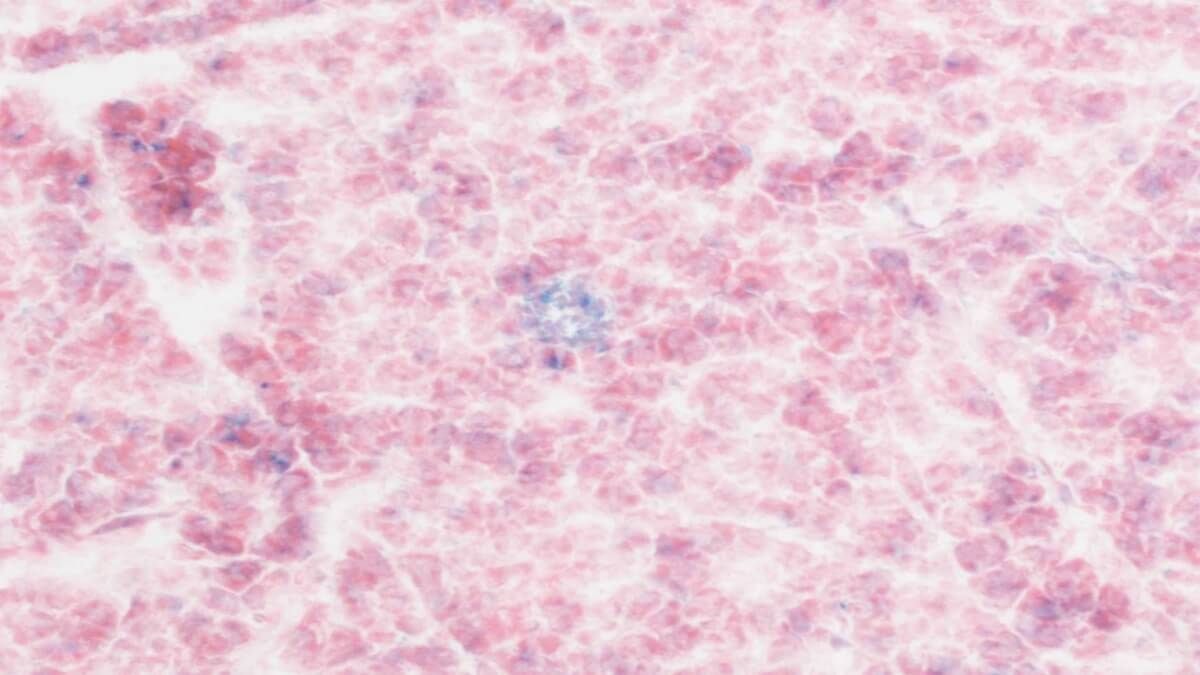
Новые методы анализа ДНК пролили свет на клеточные процессы, выявив, что восстановленная форма белка HMGB1 запускает молекулярные сигналы, известные как пути JAK/STAT и NF-κB. Эти пути тесно связаны с развитием воспаления и клеточного старения.
Когда ученые использовали существующие лекарства для блокировки этих сигнальных путей, признаки старения исчезали. Это подтвердило, что восстановленная форма HMGB1 действует именно через эти механизмы. Исследование показало, что "внеклеточный ReHMGB1, в отличие от своей окисленной формы, активно вызывал проявления старения в различных типах клеток и тканей".
Это может привести к опасному порочному кругу: с возрастом людей и увеличением числа стареющих клеток, они выделяют больше восстановленного HMGB1. Этот белок, в свою очередь, ускоряет старение здоровых клеток. Таким образом, старение может распространяться по организму через молекулярные сигналы.
Команда обнаружила, что эти клеточные эффекты имеют реальные последствия для организма животных. Введение молодым здоровым мышам восстановленной формы HMGB1 (5 мг на кг веса) привело к появлению симптомов, напоминающих старение, всего за неделю. Мышечная ткань демонстрировала повышенные маркеры старения, а анализы крови показали резкое увеличение воспалительных цитокинов, связанных с возрастом.
В другом эксперименте 15-месячным мышам с повреждениями мышц вводили антитела, блокирующие HMGB1. По сравнению с контрольной группой, мыши, получившие лечение, показали более быстрое восстановление мышц, снижение воспаления и улучшение физической активности. Они сильнее сжимали лапы, дольше бегали на беговых дорожках и быстрее заживали. Это свидетельствует о том, что воздействие на сигнальную систему HMGB1 помогает смягчить возрастные нарушения.
В образцах крови пожилых людей (70-80 лет) было обнаружено значительно больше восстановленной формы HMGB1 по сравнению с людьми в возрасте 40 лет. Аналогичное возрастное увеличение наблюдалось и у лабораторных мышей.

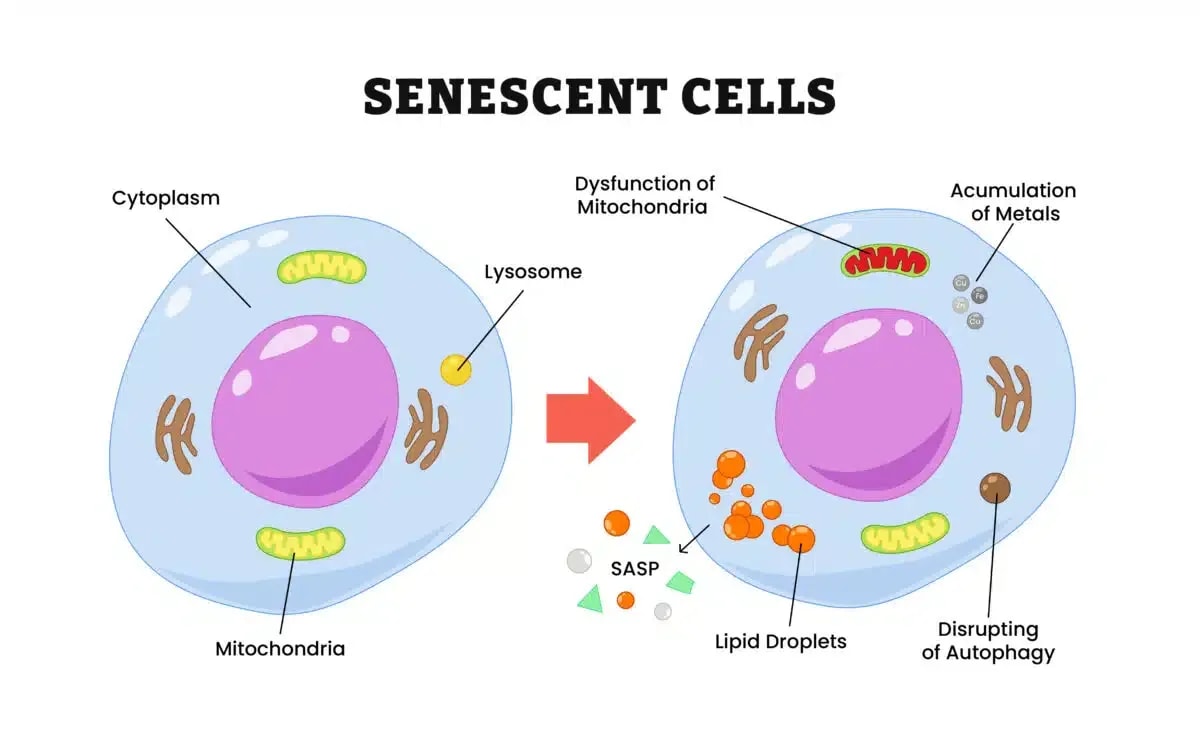
Эти открытия открывают новые возможности для создания антивозрастных препаратов. Возможны разработки, направленные на блокирование взаимодействия восстановленной формы HMGB1 с ее рецептором (известным как RAGE), улучшение ее окисления до неактивного состояния или подавление воспалительных процессов, которые она запускает.
Некоторые из этих подходов могут быть практически реализованы. Исследования показали, что момелотиниб, ингибитор JAK2, уже одобренный для лечения миелофиброза — одного из видов рака костного мозга, способен предотвращать клеточное старение, инициируемое HMGB1.
Эти открытия меняют взгляды ученых на процесс старения. Оно может быть не просто изолированным явлением в отдельных клетках, а распространяться через ткани и органы с помощью химических веществ. В исследовании восстановленная форма HMGB1 характеризуется как «прогеронийный фактор», то есть молекула, способствующая старению, и выделяется в качестве перспективной цели для будущих терапий.
Для всех, кто стремится к более грациозному старению, этот белок может стать ключевым элементом в решении проблемы и разработке новых терапевтических подходов.
Брэд Питт сможет снова сыграть в ремейке "Истории Бенджамина Баттона" главную роль через 20 лет